来源:海迈医疗
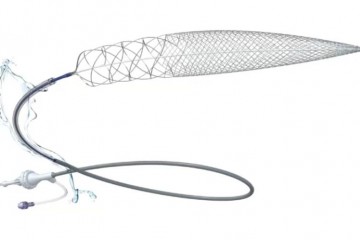
1月15日,BioBAY园内企业海迈医疗研发的首个国产完全生物型人工血管LineMatrix耐迈通®在浙江大学医学院附属邵逸夫医院临床试验入组圆满完成。

该临床试验由浙江大学医学院附属邵逸夫医院肾内科李华主任担任主要研究者,李华主任表示:“LineMatrix耐迈通®用于慢性肾衰血液透析血管通路建立以及用于自体内瘘修复的初步临床效果优异,所有患者均已顺利出院,患者启用血管移植物内瘘进行血液透析,该人工血管与自体血管相近,血管通路通畅、患者综合情况良好,我们十分期待LineMatrix耐迈通®在随访中展现出优异的预期效果,这将为国内终末期肾病患者带来新的治疗方案和选择,并大幅节省医疗支出!”
海迈医疗着眼于临床需求,开发出性能更优异的完全生物型人工血管LineMatrix耐迈通®,突破传统小口径人工血管不能快速内皮化、感染率高、通畅率低的缺陷,是目前国内唯一一家对标FDA批准的生物型人工血管技术路线的产品,未来会逐渐取代传统ePTFE人工血管,并成为自体内瘘修复方案中优于球囊和血管腔内支架的新选择。
关于海迈医疗

海迈医疗科技(苏州)有限公司成立于2021年9月1日,是一家临床阶段的创新驱动的组织工程与再生医学平台技术公司,为国内唯一、全球第二家具备量产小口径(内径≤6mm)组织工程血管能力的企业,公司创始人华中科技大学附属协和医院心脏大血管外科邱雪峰教授先后留学加州大学伯克利分校、加州再生医学研究所(CIRM)、加州大学洛杉矶分校。公司专注于利用体外生物反应器标准化大规模培养和生产小口径组织工程血管,该产品适应证包括慢性肾透析血管通路建立、下肢动脉外伤(包括战场血管损伤)血管替代、下肢动脉粥样硬化及冠状动脉搭桥术,在此技术平台上研发、生产其他再生医学产品,并扩大至全球范围的临床研究及商业化,公司过去2年内已完成4轮融资,2024年5月建成2243㎡的C+A级别GMP生产车间及质检中心并投入使用。